これらの水は一定温度範囲で特定の蒸気圧を示し,加熱により明瞭な段階的脱水を示す.配位水は結晶中の金属イオンに配位している水をさす.硫酸銅結晶cuso 4 ・5h 2 oはcu(h 2 o) 4so 4 ・h 2 oと表され,中心の銅イオンに直接配位して錯イオンを形成している4分子の水がこれである.また,陰イオン水は硫酸銅中で硫酸イオンso 4 2- と強く結合している1分子の水がこれNo A1 Re脱臭装置内で生成した白い結晶の正体を教えてください 1115 筑波山麓 (ZWl7b25 「風林火山」さんへ。 お話の内容から、硫酸カルシウムの2水和物を主成分とする硫酸カルシウムであろうと推測いたします。析出する結晶は何g か。 76 g 《解説》蒸発させた水 g に溶けていたNaCl が結晶として析出する。 例題 硫酸銅(Ⅱ)CuSO 4 の水に対する溶解度は,60℃で40 である。今,硫酸銅(Ⅱ)五水和物 CuSO 4・5H 2 O の結晶50 g を水に溶かして60℃の飽和水溶液をつくりたい。

膽礬的功效與作用 膽礬藥用價值及副作用 膽礬圖片 養生在線
硫酸銅 結晶 形
硫酸銅 結晶 形-硫酸銅の結晶作り 化学指導法の改善 (III) 化学の授業において結晶を観察したり,作ることには意義がある。 硫酸銅五水和物の単結晶作りを試みた。 再加熱法を取り入れた冷却法で,形のよい大きな結晶を得ることができた。 また,蒸発法により時間はかかるが更に成長させたり,美しい形のものを作ることができた。 本稿では,実験を遂行していく上で大切な留意点硫酸銅の精秤(採取量) Ⓐ g 、Ⓑ 1506g 硫酸銅+秤量瓶の測定 乾燥1回目:Ⓐ g、Ⓑ g 2回目:Ⓐ g、Ⓑ g ⇒両者ともに恒量がとれた。 したがってそれぞれの減少量はⒶ g、Ⓑ gとなった。 Ⓐ:4分子結晶水の重量百分率(%)=減少


硫酸铜结晶 腾讯视频
性質 化学組成は硫酸銅(ii)の5水和物(cuso 4 ・5h 2 o)であり、水によく溶ける。 加熱すると結晶水を失って白色粉末になる。 結晶系は三斜晶系。 大型の単結晶は稀で、銅鉱山の坑道の天井に鍾乳石様の塊を形成したり、内壁から霜柱状の結晶が成長するという産状が多い。硫酸銅(II)五水和物1.25g加熱したところ、 結晶水の一部が離脱して0.gの粉末が残った。 この粉末の化学式をかけ。 とい 質なお、通常、硫酸銅とは、硫酸銅(Ⅱ)五水和物(cuso 4 ・5h 2 o)のことを指すことがほとんどです。この水和物は三斜晶系結晶で、深い青色の美しい結晶として知られています。
Nov 05, 18 · 硫酸銅は中学校や高校の理科や化学の実験で目にしたことがある人が多い物質なのではないでしょうか。 青い結晶または水溶液で非常に美しいですが、食品添加物として利用されるにしてはどくどくしい見た目をしていますね。硫酸銅五水和物中を酸化銅に変え、精秤することで、硫酸銅中の銅の含有率を定量し、重量分析方法を理解する。 4週 2. 重量分析25:硫酸銅結晶中の結晶水の定量2,レポート作成指導4,硫酸銅結晶中の銅の定量5 3. 酸塩基滴定36:酸塩基反応と硫酸銅の製法 硫酸銅は、濃硫酸に銅くずを溶かしててつくりますが工業的には銅の精練のときの副産物として、たくさんつくられています。 硫酸銅の性質 硫酸銅五水和物は、水をふくんだ結晶で美しい青い色をしています。
硫酸イオン(SO42)から見れば、硫酸イオン(SO42)には二つの銅イオンが結合しています。 詳しくは、下記のJPEGファイルを開いてご覧ください。 (Cu(H2O)4SO4Cu(H2O)4Cu(H2O)4)∞と無限に繋がっていることが分かります。 またそれ以外に、どことも結合していない結晶水(H2O)もいることが分かります。 すなわち、教科書等ではよくCuSO4•5H2Oと表記されますが、 実際硫酸銅(Ⅱ)と硝酸カリウムの混合液の再結晶 実験マニュアル 使用薬品,器具,操作,失敗しない方法の説明 素材のご利用方法 教育機関以外でのご利用の場合は、「成果物利用申請」が必要です。過濾出硫酸銅結晶,將結晶置於室溫中22小時使其多餘水份自然蒸發,再精秤硫酸 銅結晶(含燒杯)重。 2、探討溫度及乙醇對硫酸銅結晶的影響 硫酸銅結晶之研究 5 配置1M 硫酸銅水溶液250 mL,並測其pH 值,接著分別取 mL 硫酸銅水溶液至編


硫酸铜结晶图片 搜狗图片搜索


五水硫酸铜 淄博永泰达化工有限公司
硫酸銅結晶 乾燥した硫酸銅(CuSO4)は白い粉末ですが、水に溶かすと青色になります。 無水物は白色粉末で,吸湿性が強く,水分を吸収して青色の水和物になるため,無水物は微量の水の検出や脱水剤に利用されます。 水を含んだ硫酸銅の青い結晶は、5個の水分子を含んだ硫酸銅(II)五水和物です:CuSO4・5H2OまたはCu(H2O)4SO4・H2O。 水和物を熱すると、水和水が段階硫酸銅の種結晶が大きくなった理由 硫酸銅水溶液の水分が蒸発することにより水溶液中の濃度が上がり、濃くなった分が 種結晶と結合し、それが繰り返されることで大きくなる。 結成と構造について 結晶学上では、鉱物が形成する結晶の姿を次の7つに分類している。問題 硫酸銅の溶解度は40℃で223g(100g溶液)である。 40℃の水100gに結晶の硫酸銅五水和物は何g溶けるか求めなさい。 解答 26g 非常に単純な問題なのですが、私が解くと"535g"になります。 参考書には解答しか書いていないため、どこがまずいのかわかり


五水硫酸铜结晶水含量的测定 综合实验 实验报告 18最新福利片在线 欧洲女性大阴口 韩国电视剧18最新 三级香港magnet 18年最好看的大片视频



Kirns Chemical Ltd Animal Feeds Fertilizer Construction Mining Water Treatment
硫酸銅(i) 化学式cu 2 so 4 。酸化銅(i)と硫酸ジメチルとの反応で合成される。無色の結晶性固体。水と作用すると直ちに加水分解して,銅,硫酸銅(ii),酸化銅(ii)を生ずる。したがって水溶液中でこれを合成することはできない。 硫酸銅(ii) 化学式cuso 4 。無水硫酸銅ともいう。化学 硫酸銅結晶の飽和水溶液 こんばんは 高校二年生です。 今、無機化学実験で 亜鉛から酸化亜鉛を 生成する実験を行っているのですが、 硫酸銅結晶30gの飽和水溶液というのは 何ミリリットル 質硫酸銅(CuSO4) 性質 ・比重 無水物 360 5水和物 229 ・無水物は白色粉末 ・水和物は青色の結晶の形を持つ固体 ・水溶液は酸性を示す ・無水物に少量の水で湿り気を与えると発熱する。 ・



硫酸铜的用途


硫酸铜结晶 哔哩哔哩 つロ干杯 Bilibili
硫酸銅めっきにおいて,これ ら結晶状態とめっき浴成分や条件との関係を調査した報告が 成されているが,必ずしも十分とは言えない。また実際のめっ き剥離に影響する反りと結晶状態との関係も不明中国で 硫酸銅の結晶 工場、あなたから直接製品を購入することができます 硫酸銅の結晶 工場のリストを表示して下さい。私たちはあなたのサードパーティの検査官によって検証信頼できる中国 硫酸銅の結晶 工場/メーカー、サプライヤー、輸出業者やトレーダーの偉大なリストを提供してい1 粉末銅0.5gを50mLのビーカーに入れ,6mol/L硫酸H 2 SO 4 10mLと10%過酸化水素水H 2 O 2 5mLを加え,穏やかに加熱する。 粉末銅が残っていれば,さらに少量の過酸化水素水を加える。


五水硫酸铜 淄博永泰达化工有限公司


硫酸铜 Cuso4 5h2o 五水硫酸铜
無水硫酸銅(CuSO 4)は、水(h 3 O)に溶解すると、硫酸銅(CuSO 4・5h 3 O)の結晶を形成する。硫酸銅とボルドーの混合物の使用方法と使用方法を調べます。 科学論文では、これらの結晶は青い五水和物と呼ばれています。本実験は、銅線から結晶硫酸銅を合成し、その収率を求めること、合成した結晶硫酸銅の実験式を求め、正しく合成が行われたことを確認することを目的としたものである。 緒言 硫酸銅とは 再結晶の原理 結晶について キレート滴定法について 実験 Ⅰ 結晶硫酸銅の合成 Ⅱ 結晶硫酸銅中の浴から得られた銅めっき皮膜の室温中での硬度及び導 電性の経時変化について検討した結果を報告する。 2.実験方法 21 めっき浴組成及び電解条件 本研究で用いためっき浴の組成及び電解条件を表1 に示す。めっき浴の建浴には硫酸銅五水和物と硫酸(い


硫酸铜结晶花 第1页 要无忧健康图库



簡析硫酸銅 Cuso4 5h2o 在水產養殖上的應用
硫酸銅水溶液を冷やし、再結晶を行いました。 すると、析出したのは、硫酸銅ではなく、 硫酸銅五水和物 の結晶だったのです。 これまでの再結晶の計算では、溶質だけが結晶になっていました。


硫酸铜结晶图片 搜狗图片搜索



蓝色结晶硫酸铜 Buy 硫酸铜 蓝晶硫酸铜 蓝晶硫酸铜product On Alibaba Com



硫酸铜结晶图片 第1页 一起扣扣网


硫酸銅晶體的結構探討 內容更正和進階探討 施建輝 臺灣化學教育


游泳池硫酸铜的作用和用法 行业知识 杭州三思泳池设备工程有限公司


硫酸铜粉末晶体结晶溶液农用杀菌剂蓝矾游泳池除藻剂水产养殖 50g 袋 高含量99 9 硫酸铜 图片价格品牌报价 京东



硫酸铜 无机化合物 搜狗百科



連毅科技 產品介紹


我的藍色寶石夢 硫酸銅結晶 Zfangの科學小玩意



硫酸铜结晶体图片 第1页 一起扣扣网



硫酸銅 珀裕企業有限公司



硫酸銅で綺麗な結晶を作ってインテリアにする方法 ぴゃかじてん



結晶實驗硫酸銅98 江銅五水硫酸銅晶體膽礬分析純殺菌滅藻


我的藍色寶石夢 硫酸銅結晶 Zfangの科學小玩意



初中化學 飽和溶液與不飽和溶液 維基教科書 自由的教學讀本



我的藍色寶石夢 硫酸銅結晶 Zfangの科學小玩意



在家也能製造 寶石 要不要試試 科學diy 每日頭條


硫酸铜晶体的制作方法是什么 有什么用途 化工资讯网


硫酸铜结晶 腾讯视频



硫酸銅結晶水加熱前 Tableware Bowl



五水硫酸銅晶體是熱飽和溶液冷卻析晶好還是蒸發析晶好 Getit01



硫酸铜不能随便用 要注意这六大事项



特色課程 藍色硫酸銅結晶 Exo Aliee



大硫酸銅晶體照片檔及更多化學照片 Istock



硫酸銅 硫酸銅晶體 顏色 用途 化學式 恒億化工 Manbetx安全 App1manbetxnet Manbet 手机版登陆


硫酸铜结晶 腾讯视频


硫酸銅の結晶といえば



硫酸銅の結晶 の写真素材 イラスト素材 アマナイメージズ



硫酸銅結晶機



Crystals Of Blue Vitriol Copper Sulfate Stock Photo Picture And Royalty Free Image Image



五水合硫酸铜 维基百科 自由的百科全书



Crystals Of Blue Vitriol Copper Sulfate Stock Photo Picture And Royalty Free Image Image


我的藍色寶石夢 硫酸銅結晶 Zfangの科學小玩意



硫酸銅晶體的結構探討 內容更正和進階探討 施建輝 臺灣化學教育


五水硫酸铜 邹平县长山福利化工厂


无水硫酸铜无水硫酸铜跟cuso4 5h2o有何不同 朵拉利品网



硫酸铜结晶图片 第1页 一起扣扣网



硫酸銅晶體硫酸銅晶體的結構探討 施建輝 Dnfiyv



硫酸硫酸銅的藍色晶體在白色背景上分離照片檔及更多化學照片 Istock



硫酸铜库存照片 图片包括有亚铁 含毒物 结晶 水晶 实验室 对象 精采 玻璃 豪华



硫酸銅晶體的結構探討 內容更正和進階探討 施建輝 臺灣化學教育


迷你硫酸铜结晶树 用硫酸铜在家做工艺品4 哔哩哔哩 つロ干杯 Bilibili



硫酸銅結晶實驗 Youtube


硫酸銅 五結晶水 Usp級 1kg 4kg 農用水族殺菌 減加壹原料館 蝦皮購物



Cu 24 肥料使用硫酸铜五水合物晶体的蓝色 Buy 硫酸铜晶体 硫酸铜的用途 硫酸铜的颜色product On Alibaba Com


美丽的硫酸铜晶体 科普中国


硫酸铜结晶 腾讯视频


我的藍色寶石夢 硫酸銅結晶 Zfangの科學小玩意



结晶水合物 维基百科 自由的百科全书



硫酸铜结晶玫瑰图片 第1页 图说健康



膽礬的功效與作用 膽礬藥用價值及副作用 膽礬圖片 養生在線


美丽的硫酸铜晶体 科普中国


美丽的硫酸铜晶体 科普中国


硫酸铜结晶机 Hqj型回转式强制结晶机


硫酸铜晶体制备方法 硫酸铜晶体制备注意事项 恒亿化工



硫酸銅晶體的結構探討 內容更正和進階探討 施建輝 臺灣化學教育



高中化学三定量实验之硫酸铜结晶水测定 哔哩哔哩 つロ干杯 Bilibili



大三男生自製 硫酸銅晶體玫瑰 送全班女生 每日頭條


美丽的硫酸铜晶体 科普中国
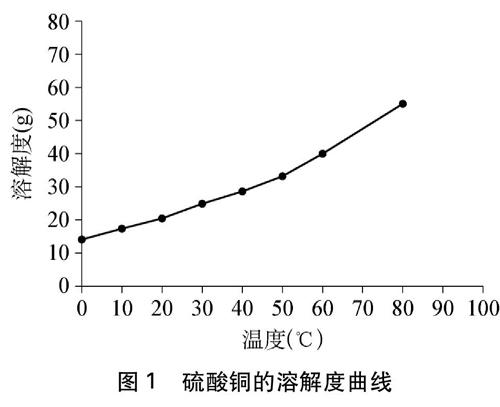


硫酸铜结晶的趣味实验设计 参考网



探索科學教育中心esec 結晶 就像藍寶石的硫酸銅晶體 讓小朋友埋下晶種 一天一天緩慢結晶長大 原來結晶是這一回事 Facebook


我的藍色寶石夢 硫酸銅結晶 Zfangの科學小玩意


五水硫酸铜 郑州德毅水处理材料有限公司


硫酸铜结晶 腾讯视频


新手 在家结晶硫酸铜 哔哩哔哩 つロ干杯 Bilibili



硫酸銅晶體的結構探討 施建輝 臺灣化學教育



帝一化工 硫酸銅 五結晶水 工業級 500g 五水合硫酸銅藍礬膽礬電鍍防腐劑第一化工 露天拍賣


硫酸铜厂家 介绍硫酸铜 性能 用途 郑州广辰首页 河南氧化铬绿厂家 铬粉批发 郑州铬酸酐供应商 超精细氢氧化铝哪家好 湖南金红石钛白粉供货商 湖北硫酸铜 销售商 河北白油 电镀添加剂 安徽氧化铬绿 环己酮经销商 陕西硬脂酸 天津元明粉直销



四幸丸 硫酸銅 硫酸銅晶體的顏色變化與它的吸放熱反應 Youtube



怎样制作硫酸铜晶体 知乎



高中化学三定量实验之硫酸铜结晶水测定 哔哩哔哩 つロ干杯 Bilibili



硫酸銅 維基百科 自由的百科全書



硫酸铜结晶图片 第1页 一起扣扣网



硫酸铜结晶失败 第1页 图说健康



硫酸铜结晶失败 第1页 图说健康


我的藍色寶石夢 硫酸銅結晶 Zfangの科學小玩意


硫酸铜 硫酸铜 淮南德比水处理科技有限公司



京楽堂 على تويتر 硫酸銅結晶ですかね


微实验 从零开始的硫酸铜结晶 哔哩哔哩 つロ干杯 Bilibili



硫酸銅 硫酸銅和硫酸銅溶液 五水合硫酸銅 華人百科



硫酸銅 硫酸銅和硫酸銅溶液 五水合硫酸銅 華人百科



硫酸铜 银基 宏观的蓝色晶体库存照片 图片包括有水晶 宏指令 精采 特写镜头 结晶 投反对票


硫酸铜 山东飞硕化工科技有限公司



淄博厂家生产电镀级硫酸铜 五水硫酸铜 蓝矾 胆矾结晶硫酸铜 阿里巴巴



結晶實驗硫酸銅98 江銅五水硫酸銅晶體膽礬分析純殺菌滅藻



硫酸銅晶體的結構探討 內容更正和進階探討 施建輝 臺灣化學教育
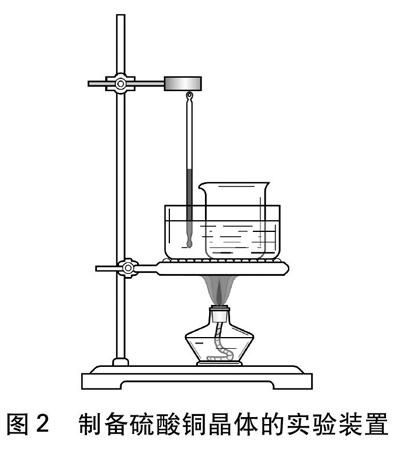


硫酸铜结晶的趣味实验设计 参考网



物質 結晶 硫酸銅 Corvet Photo Agency



硫酸銅 硫酸銅和硫酸銅溶液 五水合硫酸銅 華人百科



21 無水硫酸銅晶體人氣熱賣榜推薦 淘寶海外


0 件のコメント:
コメントを投稿